Dysbiosis and Endometriosis: The Reproductive Tract
I have a whole chapter in my new book titled “Endo’s Secret Little BIG Trigger: Bacteria”. In fact, it may be the most potent trigger of endometriosis you’ve never heard of, in some ways the “smoking gun” behind the continuous inflammation that drives endo. There is an intricate relationship between bacterial imbalances (known as dysbiosis) and endometriosis establishment, progression, immune dysfunction, and endo symptoms. Basically, it may be tied to every aspect of our endo for some of us.
While we often hear about the gut and bacteria, today I want to talk about another site rarely mentioned to us: the reproductive tract. Here, research shows the average endo sufferer may have fewer gram-positive bacteria (think of these as the “good guys”) and more gram-negative bacteria, such as E.coli or Strep (considered the “bad guys” when there are too many). While gram-negative bacteria aren’t totally bad, per-se, we want their populations kept to a minimum since a) they take up space that should be used by beneficial bacteria, and b) they produce a toxic and highly inflammatory compound called lipopolysaccharide (LPS).
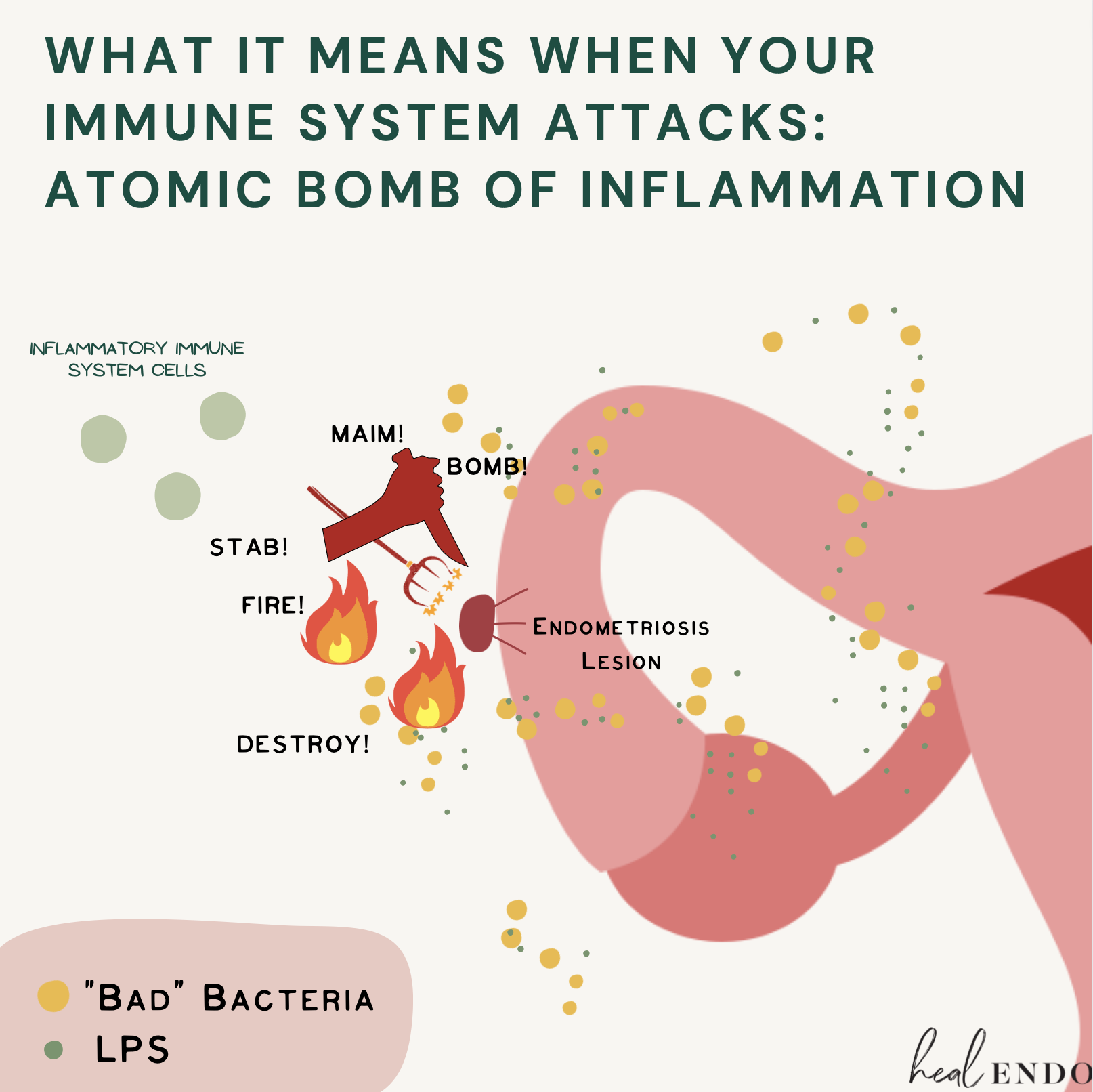
LPS is something the immune system despises. If your immune system encounters it outside of the digestive tract, it will attack that LPS with an enormous inflammatory response. ENORMOUS! Your immune system is smart, and knows LPS (and pathogenic bacteria) should not, absolutely not, be hanging out around inside your body, potentially leading to infection. Nope. And it will nuke it on site.
Alas…alas… if you have endo I’m sorry to say it’s highly likely you have lots of LPS and pathogenic bacteria hanging out in and around your reproductive tract. Research shows that for us with endo, we may have so many “bad guys” that they may dominate our microbial communities. For example, endo sufferers have been observed to have the following:
Inflammatory microbe populations in the uterus and peritoneal fluid;
A significantly altered cervical microbiome;
More Strep in their cervical mucus;
Higher concentrations of E. coli in their peritoneal fluid;
4 to 6x more E. coli in their menstrual blood; and
Higher levels of Streptococcus and E. coli in the endometrium.
With this high level of gram-negative bacteria seemingly everywhere throughout the reproductive tract, it may not come as a surprise to know that we endo sufferers altogether end up having higher concentrations of LPS in our peritoneal cavity (this is the fancy term for the inside of your abdomen but the outside of your organs, and yes, exactly where most of us have active endo lesions). This is deeply problematic, since the immune system will now expedite a enormous inflammatory response to endo-site ground zero. (1-7)
Reproductive Tract Dysbiosis + Retrograde Menstruation = Bacterial Onslaught and Chronic, Unceasing, Unrelenting, Unending Inflammation (sorry for the drama)
How did bacteria and LPS from the reproductive tract end up in the peritoneal cavity, coating your endo lesion and inviting a huge immune response? Retrograde menstruation is one way.
Retrograde menstruation is the back-flow of a small amount of menstrual blood into the peritoneal cavity that happens at menses. It’s actually totally normal, but it poses a huge problem when the blood and tissue being expelled from the uterus are saturated in pathogenic bacteria and LPS (as ours is more likely to be). The constant contamination of the peritoneal cavity with LPS will lead to an inflammatory attack with each menstrual cycle.
Letʻs do the math: every 3 weeks you bleed for one week. If this is flooding your peritoneal cavity with bacteria, your immune system will BLITZ until itʻs gone. But the BLITZ itself causes some damage too, so that damage needs some inflammation as well. But oh look, itʻs time for menstruation again! This cycle is now chronic inflammation—inflammation without end—and here your endo thrives. Why?
Inflammatory factors are what establish endometriosis in the first place, establishing blood and nerve supply (hooking these bad gals up to an IV drip of nutrients). (read here)
Chronic inflammation is what seals the deal with scar tissue and adhesions, the result of a prolonged inflammatory attack without end. (read here)
Inflammatory factors are even what provoke endo to make boatloads of estrogen. While while endo tissue may make a teeny bit more estrogen on its own (in an inflammation free environment), it may make up to 48 times more estrogen when provoked by inflammation! This is how the immune response may actually be more implicated than we realize in creating the enormous estrogen “avalanche” that endo is famous for. Without inflammation stimulating your endo, you could have 48 times LESS estrogen provoking the growth and progression of lesions in the environment surrounding your endo. (8-11)
To be clear, this is not to say stopping periods is the answer. Rather, the key is to address the infections and overgrowth in reproductive tract.
Reproductive tract dysbiosis may be a big factor when it comes to infertility, something that up to a third of women with endo may deal with at some point (of note, “infertility” does not mean you can’t have children, but rather refers to someone who has tried to conceive for over a year with no success). In fact, one study demonstrated that nearly half of women with both endometriosis and infertility issues also had chronic endometritis, an acute and prolonged infection of the endometrial lining. Endometritis is associated with recurrent miscarriages, as well as with the same strains of bacteria associated with endometriosis. Because nearly half of infertile endo patients may be dealing with this infection, I believe it’s important to investigate. In this case, a simple antibiotic treatment could dramatically improve fertility.
Even if you don't have a diagnosable infection like endometritis, you may have a subclinical infection (basically some serious dysbiosis), as 81.5 percent of women with endo were shown to have uterine pathogenic bacterial colonization to some degree! These high amounts of pathogenic bacteria will produce LPS, which can directly cause endometrial or tubal damage, prevent implantation, reduce sperm motility, and even kill sperm. In an IVF study analyzing successful outcomes, women with less LPS in the reproductive tract were much more likely to have a successful embryo transfer than those with more LPS. The connection is so powerful that I always remind folk to be extra careful with pregnancy precautions during a bacterial balancing protocol. As the bacteria become more balanced, this seems to be the time when surprises most often happen—as has happened with my clients and even with me for my happy surprise second child. Healing the microbiome is a top priority for infertility cases. (12-15)
It May Even Help Create an Endo-Like Cell
A month ago I wrote a blog about the many factors that come into play for the creation of an endo-like cell (read it here). It’s kind of like an endometrial cell, but different, and not in a good way. One of the factors that pushes these odd behaviors to surface is the constant exposure of a normal endometrial cell to chronic inflammation. When this happens, our normal endometrial cells have a last-ditch epigenetic survival tactic: turning into a mesenchymal cell that has endo-like behaviors: increased invasiveness into small nooks and crannies, an enhanced ability to migrate around the body, and even more resistance to cellular death. This is why chronic inflammation may be another prerequisite for the early development of an aggressive endo-like cell.
This may be why you’re three times more likely to develop endometriosis in the first place if you have Pelvic Inflammatory Disease (PID), an infection of the peritoneal fluid within the pelvis. Or, why our risk of developing endo is significantly increased by having genital infections. Basically, if you have dysbiosis within the uterus, it will prompt inflammation. If you never address that dysbiosis, it will become chronic inflammation. Now you have chronic inflammation inside the uterus, and your endometrial cells may start acting…insane. (16-19)
Mend the Microbes, Heal Endometriosis
Dysbiosis of the reproductive tract can make things painful, irritated, itchy, smelly, and uncomfortable. It can make sex painful, and is perhaps be the reason behind those recurrent UTIs or yeast infections. On the other hand, you may have no obvious genital symptoms but find yourself struggling with infertility, pelvic pain, or terribly painful periods as a result of bacterial reflux into the peritoneal cavity, where it stokes a wildfire of inflammation every month. It can also be SILENT. So even if you don’t have outward symptoms, please be aware you too may be suffering from dysbiosis in the nether regions if you have endometriosis.
That’s why you have a new goal: Stop all LPS and pathogenic bacteria from ever getting into the peritoneal cavity. If you do this, you may significantly reduce the amount of cyclical, chronic inflammation in your pelvis.
The good news is, reproductive tract dysbiosis can be addressed, which may not only help to reduce symptoms but also perhaps how your endometriosis behaves. With that inflammation-provoking bacteria gone, some of your endo symptoms may also be alleviated, and we will be one step closer to helping re-regulate the immune environment … and perhaps even reduce our endometriosis load.
I bet you’re excited to know where to start!!!! But, you’ll have to wait for Part 2, coming soon :) We’ll discuss a simple at home test that’s SUPER CHEAP, a few things to do, a few things to avoid, and a more pricey test that is actually really cool (and I’ll show you my results).
1 Laschke, M. W., & Menger, M. D. (2016). The gut microbiota: a puppet master in the pathogenesis of endometriosis?. American journal of obstetrics and gynecology, 215(1), 68.e1–68.e684. https://doi.org/10.1016/j.ajog.2016.02.036
2 Leonardi, M., Hicks, C., El-Assaad, F., El-Omar, E., & Condous, G. (2020). Endometriosis and the microbiome: a systematic review. BJOG : an international journal of obstetrics and gynaecology, 127(2), 239–249. https://doi.org/10.1111/1471-0528.15916
3 Koninckx, P. R., Ussia, A., Tahlak, M., Adamyan, L., Wattiez, A., Martin, D. C., & Gomel, V. (2019). Infection as a potential cofactor in the genetic-epigenetic pathophysiology of endometriosis: a systematic review. Facts, views & vision in ObGyn, 11(3), 209–216.
4 Khan, K. N., Kitajima, M., Hiraki, K., Yamaguchi, N., Katamine, S., Matsuyama, T., Nakashima, M., Fujishita, A., Ishimaru, T., & Masuzaki, H. (2010). Escherichia coli contamination of menstrual blood and effect of bacterial endotoxin on endometriosis. Fertility and sterility, 94(7), 2860–3.e33. https://doi.org/10.1016/j.fertnstert.2010.04.053
5 Khan, K. N., Fujishita, A., Kitajima, M., Hiraki, K., Nakashima, M., & Masuzaki, H. (2014). Intra-uterine microbial colonization and occurrence of endometritis in women with endometriosis. Human reproduction (Oxford, England), 29(11), 2446–2456. https://doi.org/10.1093/humrep/deu222
6 Ata, B., Yildiz, S., Turkgeldi, E., Brocal, V. P., Dinleyici, E. C., Moya, A., & Urman, B. (2019). The Endobiota Study: Comparison of Vaginal, Cervical and Gut Microbiota Between Women with Stage 3/4 Endometriosis and Healthy Controls. Scientific reports, 9(1), 2204. https://doi.org/10.1038/s41598-019-39700-6
7 Koninckx, P. R., Ussia, A., Tahlak, M., Adamyan, L., Wattiez, A., Martin, D. C., & Gomel, V. (2019). Infection as a potential cofactor in the genetic-epigenetic pathophysiology of endometriosis: a systematic review. Facts, views & vision in ObGyn, 11(3), 209–216.
8 Qi, Q., Liu, X., Zhang, Q., & Guo, S. W. (2020). Platelets induce increased estrogen production through NF-κB and TGF-β1 signaling pathways in endometriotic stromal cells. Scientific reports, 10(1), 1281. https://doi.org/10.1038/s41598-020-57997-6
9 Noble, L. S., Takayama, K., Zeitoun, K. M., Putman, J. M., Johns, D. A., Hinshelwood, M. M., Agarwal, V. R., Zhao, Y., Carr, B. R., & Bulun, S. E. (1997). Prostaglandin E2 stimulates aromatase expression in endometriosis-derived stromal cells. The Journal of clinical endocrinology and metabolism, 82(2), 600–606. https://doi.org/10.1210/jcem.82.2.3783
10 Delvoux, B., Groothuis, P., D’Hooghe, T., Kyama, C., Dunselman, G., & Romano, A. (2009). Increased production of 17beta-estradiol in endometriosis lesions is the result of impaired metabolism. The Journal of clinical endocrinology and metabolism, 94(3), 876–883. https://doi.org/10.1210/jc.2008-2218
11 Bulun, S. E., Monsavais, D., Pavone, M. E., Dyson, M., Xue, Q., Attar, E., Tokunaga, H., & Su, E. J. (2012). Role of estrogen receptor-β in endometriosis. Seminars in reproductive medicine, 30(1), 39–45. https://doi.org/10.1055/s-0031-1299596
12 Cicinelli, E., Trojano, G., Mastromauro, M., Vimercati, A., Marinaccio, M., Mitola, P. C., Resta, L., & de Ziegler, D. (2017). Higher prevalence of chronic endometritis in women with endometriosis: a possible etiopathogenetic link. Fertility and sterility, 108(2), 289–295.e1. https://doi.org/10.1016/j.fertnstert.2017.05.016
13 Cicinelli, E., Matteo, M., Tinelli, R., Pinto, V., Marinaccio, M., Indraccolo, U., De Ziegler, D., & Resta, L. (2014). Chronic endometritis due to common bacteria is prevalent in women with recurrent miscarriage as confirmed by improved pregnancy outcome after antibiotic treatment. Reproductive sciences (Thousand Oaks, Calif.), 21(5), 640–647. https://doi.org/10.1177/1933719113508817
14 Khaleque Newaz Khan, Akira Fujishita, Michio Kitajima, Koichi Hiraki, Masahiro Nakashima, Hideaki Masuzaki. (2014). Intra-uterine microbial colonization and occurrence of endometritis in women with endometriosis. Human Reproduction. 29(11), 2446–56. https://doi.org/10.1093/humrep/deu222
15 Deb K, Chatturvedi M, M, Jaiswal Y, K. (2004). Gram-Negative Bacterial Endotoxin- Induced Infertility: A Birds Eye View. Gynecol Obstet Invest 57, 224-32. https://www.doi.org/10.1159/000076761
16 Wu, M. H., Hsiao, K. Y., & Tsai, S. J. (2019). Hypoxia: The force of endometriosis. The journal of obstetrics and gynaecology research, 45(3), 532–541. https://doi.org/10.1111/jog.13900
17 Kalluri, R., & Weinberg, R. A. (2009). The basics of epithelial-mesenchymal transition. The Journal of clinical investigation, 119(6), 1420–1428. https://doi.org/10.1172/JCI39104
18 Tai, F. W., Chang, C. Y., Chiang, J. H., Lin, W. C., & Wan, L. (2018). Association of Pelvic Inflammatory Disease with Risk of Endometriosis: A Nationwide Cohort Study Involving 141,460 Individuals. Journal of clinical medicine, 7(11), 379. https://doi.org/10.3390/jcm7110379
19 Lin, W. C., Chang, C. Y., Hsu, Y. A., Chiang, J. H., & Wan, L. (2016). Increased Risk of Endometriosis in Patients With Lower Genital Tract Infection: A Nationwide Cohort Study. Medicine, 95(10), e2773. https://doi.org/10.1097/MD.0000000000002773